کاربرد نانومواد در الکتروشیمی (4/1)
4- برچسب گذاری زیست مولکولها(Labeling Biomolecules)
نانومواد به طور گسترده به عنوان برچسب و ردیاب1 زیست مولکولها برای زیست حسگر الکتروشیمیایی از سال 2000 استفاده شده اند(1). برچسب گذاری زیست مولکولها مثل پادگن ها، پادتن ها و DNA با نانو ذرات به طور فزاینده نقش مهمی در توسعه ی زیست حسگرهای الکتروشیمیایی حساس ایفا می کند.
نانوذرات در مقایسه با برچسب های آنزیمی بسیار پایدار هستند، آنها بسیار حساس هستند (هزاران اتم می توانند از یک نانوذره رها شوند) و طیف گسترده ای از نانو ذرات، درها را برای تسهیم باز می کنند. نانوذرات امروزه به عنوان برچسب الکتروشیمیایی یا به عنوان حامل شامل چندین صد یا هزاران بر چسب الکترواکتیو و حد تشخیص پایین چند صد زیست مولکول استفاده می شوند(2). زیست مولکولهای برچسب گذاری شده با نانوذرات می توانند زیست فعالی و برهمکنش با همتایانشان را به دست آورند، و بر اساس آشکارسازی الکتروشیمیایی این نانوذرات، مقدار یا غلظت آنالیت ها تعیین شود.
انحلال برچسب نانوذرات-عمدتاً فلزی و نانوذرات نیمه هادی و اندازه گیری یونهای حل شده با ولتامتری عاری سازی یک روش عمومی الکتروآنالیز می باشد. چون این روش یک تکنیک تجزیه ای الکتروشیمیایی بسیار قوی برای اندازه گیری مقدار ناچیز فلزات می باشد.
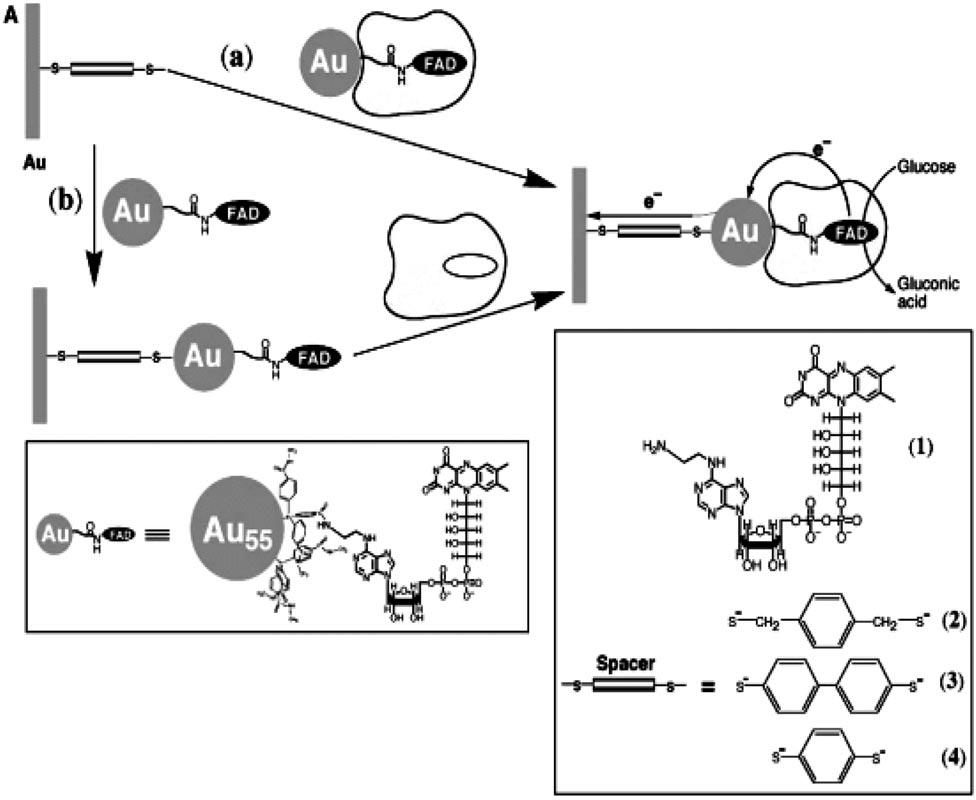
برای مثال گروه لیموجس 2یک ایمونوسنسور الکتروشیمیایی حساس برای ایمونوگلوبین G بز3 IgG بر اساس برچسب نانوذرات طلا گزارش داده است. ابتدا پادتن IgG روی یک سطح microwell تثبیت شده و با IgG بر همکنش داد تا شناسایی شود؛ سپس نانوذرات طلای بر چسب زده پادتن IgG برای مزدوج شدن به آنالیت اضافه شدند. اضافه کردن محلول برم اسیدی-برمید منجر به انحلال اکسایشی نانوذرات طلا شده و سپس یونهای طلای محلول به طور الکتروشیمیایی کاهش داده شده و روی الکترود انباشته شدند و متعاقباً توسط ولتامتری عاری سازی آندی4 با استفاده از الکترودهای نواری مبتنی بر کربن آشکار سازی شدند. ترکیب آشکارساز حساس به یونهای طلا با ولتامتری عاری سازی و رهایی تعداد زیادی یونهای طلا به محض انحلال نانوذرات طلا یک مسیر تقویتی را ایجاد میکند که آشکارسازی IgG در غلظت pM 3 را موجب می شود (شکل 1).
ایمونوسنسور مغناطیسی الکتروشیمیایی مبتنی بر نانوذره فلزی با استفاده از مهره5های مغناطیسی و برچسب نانوذره طلا توسعه یافته است. مهره های مغناطیسی آنتی-IgG اصلاح شده، به سطح مبدل خمیر کربن توسط مگنت متصل شده و در داخل حسگر تثبیت شدند. برچسب نانوذره طلا در سطح مهره های مغناطیسی توسط ایمونوسنجی ساندویچ6 در محفظه قرار گرفت. تجزیه عاری سازی الکتروشیمیایی با حساسیت بالا یک روش سریع و ساده برای تعیین کمیت ردیابهای نانوذره طلا ارائه داد. سیگنال عاری سازی نانوذرات متناسب با غلظت IgG هدف در محلول نمونه یافت شد.
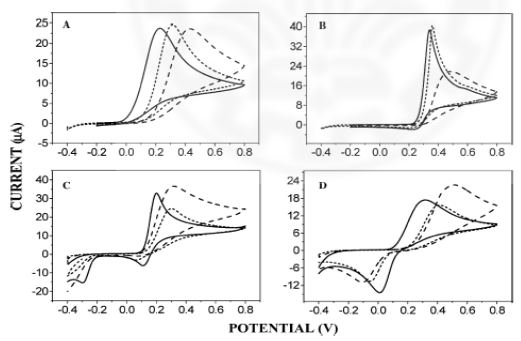
همچنین قابلیت های چندگانه ی نقاط کوانتومی در ارتباط با ایمونوسنجی به اثبات رسیده است. پروتکل ایمونوسنجی الکتروشیمیایی برای اندازه گیری های همزمان پروتئین ها بر اساس استفاده از ردیاب های نانوکریستال معدنی مختلف توصیف شده است. قابلیت آشکارسازی الکتریکی چند پروتئینی با ویژگی آمپلی فایر مبدلهای عاری سازی الکتروشیمیایی و با جداسازی های مغناطیسی موثر (برای اثرات جذب غیر ویژه) جفت شد. ایمونوسنجی ساندویچی الکتریکی چند آنالیتی شامل رویداد اتصال دوگانه، مبتنی بر پادتن های متصل شده به برچسب های نانوکریستال و مهره های مغناطیسی می باشد. پیوند کربامات7 برای مزدوج شدن نانوکریستال های هیدروکسیل- منقطع8 با پادتن های ثانویه استفاده شد. هر رویداد آشکارسازی زیستی پیک ولتامتری متمایز را بهبود بخشید، که موقعیت، اندازه، هویت و غلظت مربوط به پادگن را منعکس کرد. این قابلیت برای ایمونوسنجی همزمان B2-میکروگلوبین 9، IgG، سرم آلبومین گاوی 10 و پروتئین C- واکنشی 11در ارتباط با کریستالهای کلوئیدی ZnS، CdS، PbS و CuS، به ترتیب نشان داده شده است ( برای طرح پروتکل ببینید شکل 2).
شکل 2. پروتکل آشکارسازی الکتریکی چند پروتئینی مبتنی بر ردیابهای نانوکریستال کلوئیدی معدنی. (A) مهره های مغناطیسی اصلاح شده با پادتن (B) اتصال پادگن ها به پادتن ها روی مهره های مغناطیسی. (C) برچسب نانوکریستال پادتن های ثانویه. (D) انحلال نانوکریستال ها و آشکارسازی عاری سازی الکتروشیمیایی.منبع:
(1)
گلابی، سید
مهدی(1389)، مقدمه ای بر الکتروشیمی تجزیه: اصول و کاربردها، تبریز، انتشارات
ستوده.
(2)
Martin Pumera, Samuel S´anchez, Izumi Ichinose, Jie Tang, "Electrochemical nanobiosensors", Sensors and Actuators B 123 (2007) 1195–1205
- ۰ نظر
- ۰۲ فروردين ۹۴ ، ۱۴:۴۹